Expertise
Der Mehrwert unseres eQMS nach 13485 im Entwicklungsprozess
Wer Produkte in der Medizintechnik entwickelt, kennt die Realität:
Ideen allein reichen nicht.
Zwischen der ersten Produktidee und einem marktfähigen Medizinprodukt liegen regulatorische Anforderungen, Dokumentationspflichten, Risikomanagement und Audits. Entwicklung findet deshalb nicht nur im Labor oder im Designdienstleister statt – sondern immer auch innerhalb eines regulierten Systems.
Für Unternehmen bedeutet das vor allem eines:
Sie brauchen Partner, die sich in diesem Umfeld sicher bewegen können. Genau aus diesem Grund haben wir unsere Arbeitsweise konsequent darauf ausgerichtet, Teil dieses Systems zu sein.
Wir haben früh festgestellt:
Effiziente Entwicklung ist nur dann möglich, wenn sich alle Beteiligten reibungslos in bestehende regulierte Prozesse einfügen können. Ein Designbüro, das losgelöst von Design Controls, Risikomanagement und Dokumentationsanforderungen arbeitet, erzeugt Mehraufwand. Im schlimmsten Fall sogar regulatorische Risiken.
Wenn Produktkomplexität Planungssicherheit braucht
Viele der Unternehmen, mit denen wir arbeiten, sind mittelständische MedTech-Hersteller. Sie entwickeln hochkomplexe Produkte, oft über mehrere Jahre hinweg und mit vielen beteiligten Disziplinen. In solchen Projekten ist ein externer Entwicklungspartner nicht einfach nur ein kreativer Impulsgeber. Er muss sich in bestehende Prozesse integrieren können – technisch, organisatorisch und regulatorisch. Genau hier entsteht häufig Reibung.
Wenn externe Partner anders arbeiten als interne Entwicklungsteams, entstehen zusätzliche Schnittstellen:
Dokumentation muss nachträglich angepasst werden, Entscheidungen sind schwer nachvollziehbar oder Prozesse passen nicht zusammen.
Unser Ansatz war deshalb von Anfang an klar:
Wir wollten so arbeiten, dass wir ohne Reibungsverluste Teil des Entwicklungsökosystems unserer Kunden werden können.
Deshalb orientieren sich unsere Designprozesse an den Strukturen regulierter Entwicklungsprojekte.
Unser QMS bietet mittelständischen MedTech-Herstellern folgendes:
- Mehr Planungssicherheit bei komplexen Entwicklungsprojekten - planbare Aufwände
- Entscheidungen sind nachvollziehbar dokumentiert-> kein unnötiges Rework
- Entwicklungsschritte sind transparent und planbar
- Schnellere und bewertbare Entscheidungen
- Nahtlose Integration in bestehende Systeme
- Designprozesse lassen sich in Design Controls einordnen
- Klare Schnittstellen zu Quality Assurance (QA) und Regulatory Affairs (RA)
- Zugang zu langjähriger Erfahrung und einem groß aufgestellten Experten-Netzwerk
Für unsere Kunden bedeutet das vor allem eines:
Planungssicherheit.
Gerade bei komplexen Produkten ist es entscheidend, dass Entwicklungspartner nicht nur kreativ arbeiten – sondern auch systemisch denken. Dazu kommt ein Faktor, der oft unterschätzt wird: Erfahrung. Seit fast 30 Jahren arbeiten wir in der Produktentwicklung der Medizintechnik. Über die Zeit ist ein großes Netzwerk aus Spezialisten, Partnern und Branchenkontakten entstanden, das wir aktiv in Projekte einbringen können.
Viele unserer Kunden schätzen genau das:
Sie arbeiten nicht nur mit einer Designagentur – sondern mit einem Entwicklungspartner, der das MedTech-Ökosystem versteht.

Wenn aus einer großartigen Idee ein Medizinprodukt werden soll
Eine ganz andere Situation erleben wir bei Startups und Gründern.
Hier steht am Anfang oft eine starke Idee – manchmal sogar eine technologische Innovation. Gleichzeitig ist das regulatorische Umfeld für viele junge Unternehmen Neuland. Während etablierte Unternehmen meist über eigene QA- und RA-Strukturen (Quality Assurance/ Regulatory Affairs) verfügen, stehen Startups und Gründer vor ganz anderen Herausforderungen.
Plötzlich tauchen Fragen auf wie:
- Welche Dokumentation wird überhaupt benötigt?
- Wie strukturiert man Entwicklungsprozesse richtig?
- Was erwarten Benannte Stellen oder Audits?
- Wann müssen regulatorische Anforderungen berücksichtigt werden?
In dieser Phase kann ein strukturierter Entwicklungspartner enorm helfen. Unsere Arbeitsweise gibt Startups einen klaren Rahmen, um ihre Idee systematisch weiterzuentwickeln. Unser QMS schafft für junge Unternehmen vor allem eines: Orientierung und Sicherheit.
Das bedeutet:
- Strukturierte Produktentwicklung - ein klarer Entwicklungsrahmen dabei, Ideen systematisch in ein belastbares Produktkonzept zu überführen
- Entwicklungsentscheidungen werden sauber dokumentiert
- Designprozesse sind nachvollziehbar aufgebaut
- Orientierung im regulatorischen Kontext - regulatorische Anforderungen werden früh mitgedacht
- Typische Stolpersteine können vermieden werden
- Zugang zu langjähriger Erfahrung und einem groß aufgestellten Experten-Netzwerk
Mindestens genauso wichtig ist jedoch etwas anderes:
Erfahrung und Austausch. Viele Gründer profitieren davon, einen Partner an ihrer Seite zu haben, der bereits viele MedTech-Projekte begleitet hat – und der weiß, wo Herausforderungen typischerweise entstehen. Oft entstehen daraus auch wertvolle Verbindungen: zu Experten, zu spezialisierten Partnern oder zu anderen Akteuren im MedTech-Umfeld.
Für Startups bedeutet das:
Sie gewinnen nicht nur Unterstützung im Design – sondern einen Entwicklungspartner, der ihnen hilft, sich sicher im regulierten Umfeld der Medizintechnik zu bewegen.
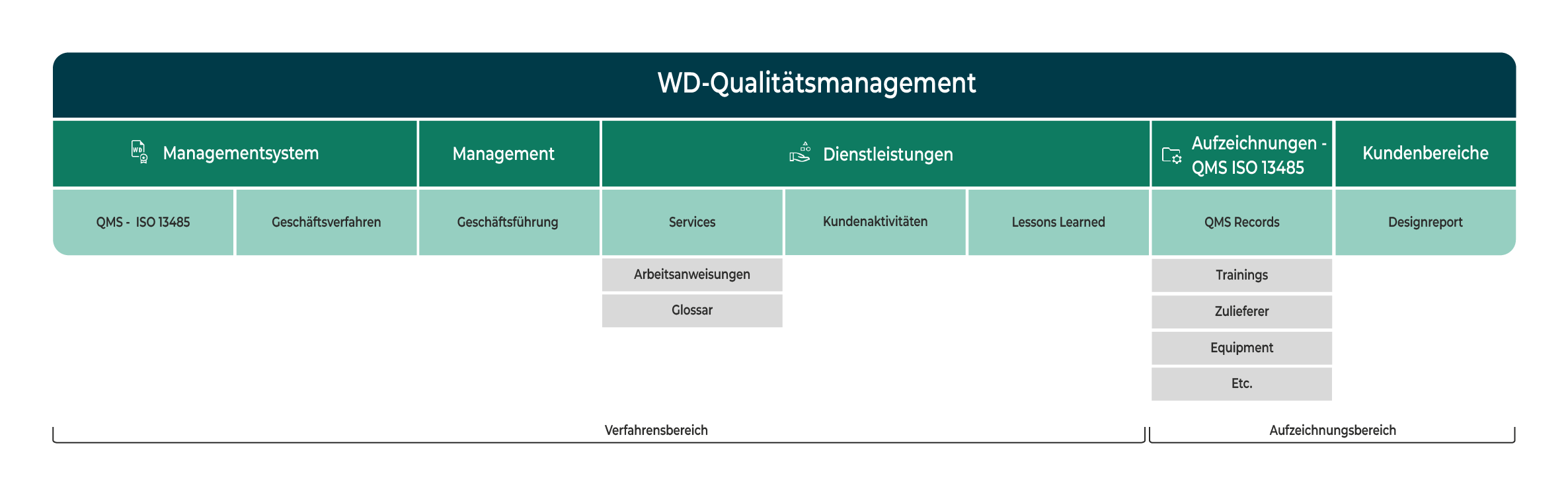
Was unser WD eQMS für uns bedeutet:
Damit diese Zusammenarbeit funktioniert, braucht es eine klare Grundlage.
Unser Qualitätsmanagementsystem orientiert sich an den Anforderungen der ISO 13485, dem zentralen Qualitätsstandard in der Medizintechnik.
Damit meinen wir:
Unsere Prozesse sind so aufgebaut, dass sie sich an den Anforderungen regulierter Entwicklungsprojekte orientieren.
Dazu gehören unter anderem:
- strukturierte Designprozesse
- klare Verantwortlichkeiten
- nachvollziehbare Dokumentation
- Traceability von Entscheidungen
- definierte Schnittstellen zu Quality Assurance (QA) und Regulatory Affairs (RA)
Gleichzeitig achten wir darauf, dass diese Strukturen praktisch funktionieren und nicht zur reinen Bürokratie werden. Denn ein Managementsystem entfaltet seinen Wert nicht durch ein Zertifikat – sondern dadurch, dass es im Alltag tatsächlich genutzt wird.
Ein Nebeneffekt: bessere Zusammenarbeit im Team
Ein strukturierter Rahmen hat nicht nur Auswirkungen auf Projekte mit unseren Kunden. Er hilft auch intern. Klare Prozesse erleichtern die Zusammenarbeit zwischen Teams, machen Wissen besser übertragbar und sorgen dafür, dass Erfahrungen aus Projekten systematisch weiterentwickelt werden können.
Für unsere Kunden bedeutet das vor allem eines:
Sie profitieren von einer Arbeitsweise, die über viele Projekte hinweg stabil und lernfähig bleibt.
Medizintechnik entsteht selten allein
Sie entsteht im Zusammenspiel von Entwicklung, Design, Regulierung und vielen beteiligten Partnern. Unser Ansatz sorgt dafür, dass wir uns genau in diesem Umfeld sicher bewegen können.
Das Ergebnis:
Weniger Rückfragen.
Weniger Missverständnisse.
Weniger Iterationsschleifen.
Weniger Rework.
Weniger Stress im Projektverlauf.
Schnellere Freigaben.
Schnellere und bewertbare Entscheidungen.
Belastbarere Ergebnisse.
Mehr Sicherheit.
Gutes MedTech-Design ist nicht nur funktional und nutzerzentriert. Es ist anschlussfähig, nachvollziehbar und regulatorisch belastbar. Und genau das spart am Ende Zeit, Kosten – und Nerven.
Häufig gestellte Fragen